ГЛАВА 6. ОБЩАЯ ХАРАКТЕРИСТИКА КОНСТРУКТИВНОГО МЕТАБОЛИЗМА ПРОКАРИОТ
Образ жизни прокариот состоит в постоянном воспроизводстве своей биомассы. Совокупность протекающих в клетке процессов, обеспечивающих воспроизводство биомассы, называется обменом веществ, или метаболизмом. Клеточный метаболизм складывается из двух потоков реакций, имеющих разную направленность: энергетического и конструктивного метаболизма. Энергетический метаболизм — это поток реакций, сопровождающихся мобилизацией энергии и преобразованием ее в электрохимическую (DmH+) или химическую (АТФ) форму, которая затем может использоваться во всех энергозависимых процессах. Конструктивный метаболизм (биосинтезы) — поток реакций, в результате которых за счет поступающих извне веществ строится вещество клеток; это процесс, связанный с потреблением свободной энергии, запасенной в химической форме в молекулах АТФ или других богатых энергией соединений.
В микробиологической литературе для обозначения энергетических и конструктивных процессов пользуются также терминами "катаболизм" и "анаболизм", имеющими отношение к распаду или синтезу органических молекул, происходящему соответственно с выделением или потреблением свободной энергии. Следует иметь в виду, что термин "катаболизм" применим для обозначения не всех типов энергетического обмена прокариот. Существуют группы прокариотных организмов, энергетический метаболизм которых не связан с превращениями органических соединений (прокариоты с фотолито- и хемолитотрофным типом энергетического обмена). По отношению к такого рода энергетическим процессам термин "катаболизм" неприменим. У этих организмов функционирует только один поток превращений органических соединений углерода — анаболический.
Метаболические пути конструктивной и энергетической направленности состоят из множества последовательных ферментативных реакций и могут быть разделены на три этапа. На начальном — воздействию подвергаются молекулы, служащие исходными субстратами. Иногда эту часть метаболического пути называют периферическим метаболизмом, а ферменты, катализирующие первые этапы превращения субстрата, — периферическими. Последующие превращения включают ряд ферментативных реакций и приводят к образованию промежуточных продуктов, или метаболитов, а сама цепь превращений объединяется под названием промежуточного метаболизма. Образующиеся на последних этапах конечные продукты конструктивных путей используются для построения вещества клеток, а энергетических — выделяются в окружающую среду.
Конструктивные и энергетические процессы протекают в клетке одновременно. У большинства прокариот они тесно связаны между собой. Однако у некоторых прокариотных организмов можно выделить последовательности реакций, служащих только для получения энергии или только для биосинтеза. Связь между конструктивными и энергетическими процессами прокариот осуществляется по нескольким каналам. Основной из них — энергетический. Определенные реакции поставляют энергию, необходимую для биосинтезов и других клеточных энергозависимых функций. Биосинтетические реакции кроме энергии нуждаются часто в поступлении извне восстановителя в виде водорода (электронов), источником которого служат также реакции энергетического метаболизма. И наконец, тесная связь между энергетическими и конструктивными процессами проявляется в том, что определенные промежуточные этапы или метаболиты обоих путей могут быть одинаковыми (хотя направленность потоков реакций, относящихся к каждому из путей, различна). Это создает возможности для использования общих промежуточных продуктов в каждом из метаболических путей. Промежуточные соединения такой природы предложено называть амфиболитами, а промежуточные реакции, одинаковые для обоих потоков, — амфиболическими.
Метаболизм прокариот, как энергетический, так и конструктивный, отличается чрезвычайным разнообразием, которое есть результат способности этих форм жизни использовать в качестве источников энергии и исходных субстратов для построения веществ тела самый широкий набор органических и неорганических соединений. Такая способность обусловлена различиями в наборе клеточных периферических ферментов, воздействующих на исходные субстраты и видоизменяющих их молекулы в направлении, позволяющем им далее метаболизироваться по каналам промежуточного метаболизма. В отличие от периферического промежуточный метаболизм прокариот не отличается существенным разнообразием, хотя сравнительно с таковым эукариотных организмов он состоит из большего числа вариантов.
ХИМИЧЕСКИЙ СОСТАВ ПРОКАРИОТНОЙ КЛЕТКИ
Химический состав клеток в принципе одинаков у всех организмов. Клетки прокариот содержат от 70 до 90% воды. Основную массу сухих веществ, на долю которых приходятся остальные 10–30%, составляют белки, нуклеиновые кислоты, липиды и полисахариды. Несколько процентов сухого вещества клеток приходится на низкомолекулярные органические вещества и соли (табл. 9).
Таблица 9. Химический состав клетки Е. coli* (по Neidhardt, 1987)
| Компонент | Общее количество, % от сухих веществ клетки | Молекулярная масса, Да | Количество молекул в клетке | Число разных видов молекул в клетке |
| Белок | 55,0 | 4,7x104 | 2 350 000 | 1850 |
| РНК | 20,5 | |||
| 23S рРНК | 1,0x106 | 18 700 | 1 | |
| 16S рРНК | 5,0x105 | 18 700 | 1 | |
| 5S рРНК | 3,9x104 | 18 700 | 1 | |
| тРНК | 2,5x104 | 198 000 | 60 | |
| иРНК | 1,0x106 | 1 380 | 600 | |
| ДНК | 3,1 | 2,5x109 | 2 | 1 |
| Липиды | 9,1 | 705 | 22 000 000 | |
| Липополисахариды | 3,4 | 4070 | 1 430 000 | 1 |
| Пептидогликан | 2,5 | (904)n | 1 | 1 |
| Гликоген | 2,5 | 1,0x106 | 4 300 | 1 |
| Полиамины | 0,4 | |||
| путресцин | 88 | 5 600 000 | 1 | |
| спермидин | 145 | 1 100 000 | 1 | |
| Метаболиты, кофакторы, ионы | 3,5 | 800 |
* Анализировали клетки Е. coli, выращенные в условиях аэрирования на синтетической среде с глюкозой при 37°; время генерации — 40 мин.
Макромолекулы, составляющие основную массу сухих веществ клетки, — полимеры, построенные из мономерных единиц. Исключением служат липиды, не являющиеся полимерами, так как молекулы в них не соединены между собой ковалентными связями. Углеводные полимеры построены на основе повторяющихся единиц одного, двух или более типов, например, запасной полисахарид гликоген, построенный из остатков глюкозы, или пептидогликан клеточной стенки, образованный чередованием N-ацетилглюкозамина и N-ацетилмурамовой кислоты. В клетке углеводные полимеры представлены часто одним видом молекулы (табл. 9).
Полимерные молекулы белков и нуклеиновых кислот синтезируются на матрице, которая и определяет последовательность составляющих их мономеров. Возможности для синтеза разнообразных по функциям и структуре клеточных метаболитов реализуются на стадии сборки полимеров путем различных сочетаний исходных строительных блоков. В основе огромного числа видо- и функционально специфических белков лежат комбинации из 20 аминокислот, а чтобы зашифровать весь объем генетической информации одной клетки или многоклеточного организма оказалось достаточным комбинации из 4 нуклеотидов.
Прокариотная клетка в норме содержит примерно 2000—2500 различных белков, каждый из которых представлен 400—1000 молекулами. Количество молекул нуклеиновых кислот каждого вида определяется их функциональным назначением: ДНК — одного вида и представлена одной или несколькими копиями; количество разных молекул РНК в клетке колеблется на несколько порядков.
ПОТРЕБНОСТИ ПРОКАРИОТ В ПИТАТЕЛЬНЫХ ВЕЩЕСТВАХ
Мономеры, необходимые для построения основных клеточных компонентов, могут быть синтезированы клеткой или поступать в готовом виде из среды. Чем больше готовых соединений должен получать организм извне, тем ниже уровень его биосинтетических способностей, так как химическая организация всех свободноживущих форм одинакова.
Источники углерода
В конструктивном метаболизме основная роль принадлежит углероду, поскольку все соединения, из которых построены живые организмы, — это соединения углерода. Их известно около миллиона. Прокариоты способны воздействовать на любое известное углеродное соединение, т. е. использовать его в своем метаболизме. В зависимости от источника углерода для конструктивного метаболизма все прокариоты делятся на две группы:
автотрофы, к которым принадлежат организмы, способные синтезировать все компоненты клетки из углекислоты, и гетеротрофы, источником углерода для конструктивного метаболизма которых служат органические соединения15. Понятия "авто-" и "гетеротрофия" характеризуют, таким образом, тип конструктивного метаболизма. Если автотрофия — довольно четкое и узкое понятие, то гетеротрофия — понятие весьма широкое и объединяет организмы, резко различающиеся своими потребностями в питательных веществах.
15 Впервые понятия "авто-" и "гетеротрофия" были введены для противопоставления растительного и животного образа жизни. Позднее их распространили на все другие организмы, в том числе и на прокариотные. Термин "автотрофия" означает питающийся самостоятельно, "гетеротрофия"—питающийся другими; от греческих слов: autos—сам, heteros— другой, trophe — пища.
Наибольшая степень гетеротрофности присуща прокариотам, относящимся к облигатным внутриклеточным паразитам, т. е. организмам, которые могут жить только внутри других живых клеток. Паразитический образ жизни привел к редукции некоторых метаболических путей у этих прокариот, что и обусловило полную их зависимость от метаболизма клетки хозяина.
Другие паразитические прокариотные организмы удается выращивать на искусственных средах, но состав таких сред необычайно сложен. Они содержат, как правило, белки или продукты их неглубокого гидролиза (пептиды), полный набор витаминов, фрагменты нуклеиновых кислот и т. д. Для приготовления питательных сред такого состава используют мясные гидролизаты, цельную кровь или ее сыворотку. Формы, способные расти при создании подходящих условий вне клетки хозяина, называют факультативными паразитами.
Следующую крупную группу прокариот составляют так называемые сапрофиты — гетеротрофные организмы, которые непосредственно от других организмов не зависят, но нуждаются в готовых органических соединениях16. Они используют продукты жизнедеятельности других организмов или разлагающиеся растительные и животные ткани. К сапрофитам относится большая часть бактерий. Степень требовательности к субстрату у сапрофитов весьма различна. В эту группу входят организмы, которые могут расти только на достаточно сложных субстратах (молоко, трупы животных, гниющие растительные остатки), т. е. им нужны в качестве обязательных элементов питания углеводы, органические формы азота в виде набора аминокислот, пептидов, белков, все или часть витаминов, нуклеотиды или готовые компоненты, необходимые для синтеза последних (азотистые основания, пятиуглеродные сахара). Чтобы удовлетворить потребность этих гетеротрофов в элементах питания, их обычно культивируют на средах, содержащих мясные гидролизаты, автолизаты дрожжей, растительные экстракты, молочную сыворотку.
Есть прокариоты, требующие для роста весьма ограниченное число готовых органических соединений в основном из числа витаминов и аминокислот, которые они не в состоянии синтезировать сами, и наконец, гетеротрофы, нуждающиеся только в одном органическом источнике углерода. Им может быть какой-либо сахар, спирт, кислота или другое углеродсодержащее соединение. Описаны бактерии из рода Pseudomonas, способные использовать в качестве единственного источника углерода и энергии любое из 200 различных органических соединений, и бактерии, для которых источником углерода и энергии может служить узкий круг довольно экзотических органических веществ. Например, Bacillus fastidiosus может использовать только мочевую кислоту и продукты ее деградации, а некоторые представители рода Clostridium растут только в среде, содержащей пурины. Использовать другие органические субстраты для роста они не могут. Биосинтетические способности этих организмов развиты в такой степени, что они сами могут синтезировать все необходимые им углеродные соединения.
16 Термин "сапрофиты" происходит от греческих слов sapros — гнилой и phyton—растение.
Особую группу гетеротрофных прокариот, обитающих в водоемах, составляют олиготрофные бактерии, способные расти при низких концентрациях в среде органических веществ. Организмы, предпочитающие высокие концентрации питательных веществ, относят к копиотрофам17. Если у типичных копиотрофов оптимальные условия для роста создаются при содержании в среде питательных веществ в количестве примерно 10 г/л, то для олиготрофных организмов — в пределах 1—15мг углерода/л. В средах с более высоким содержанием органических веществ такие бактерии, как правило, расти не могут и погибают.
17 Термины происходят от греческих слов oligos — малый и trophe — пища, латинского copia — изобилие.
Различия между гетеротрофными прокариотами с высокими потребностями в готовых органических соединениях и теми, потребности которых минимальны и сводятся, как правило, к одному какому-нибудь органическому источнику углерода, заключаются, таким образом, в степени развития их биосинтетических. способностей. Крайняя степень развития биосинтетических способностей — способность строить все клеточные компоненты из углекислоты — присуща группе автотрофных прокариот.
Как можно видеть из изложенного выше, в мире прокариот не существует резкой границы между авто- и гетеротрофными организмами, так же как нет ее в ряду одноуглеродных соединений (CO2, CO, HCOOH, НСНО, CH3OH, CH4), каждое из которых может служить источником углерода для определенной группы прокариот. Однако использование термина "автотрофия" удобно для обозначения конкретного типа конструктивного метаболизма, поскольку в процессе эволюции он оказался специфически связанным с определенными видами энергетических процессов, что привело к появлению у прокариот таких типов жизни, которые отсутствуют у более высокоорганизованных форм.
Азот
Азот (наряду с углеродом, водородом и кислородом) является одним из четырех основных элементов, участвующих в построении клетки. В расчете на сухие вещества его содержится приблизительно 10%. Природный азот бывает в окисленной, восстановленной и молекулярной формах. Подавляющее большинство прокариот усваивают азот в восстановленной форме. Это соли аммония, мочевины, органические соединения (аминокислоты или пептиды). Окисленные формы азота, главным образом нитраты, также могут потребляться многими прокариотами. Так как азот в конструктивном клеточном метаболизме используется в форме аммиака, нитраты перед включением в органические соединения должны быть восстановлены.
Восстановление нитратов до аммиака осуществляется посредством последовательного действия двух ферментов — нитрат- и нитритредуктазы. Нитратредуктаза катализирует НАД·H2-зависимое18 восстановление нитрата до нитрита:
NO3– + НАД·H2 ® NO2–+НАД++H2O,
в результате которого осуществляется перенос на NO3– двух электронов. Нитритредуктаза катализирует шестиэлектронное восстановление NO2– до NH3:
NO2– + ЗНАД·H2 + Н+ ® NH3 + 3НАД++2H2O.
18 НАД (Ф)+— окисленная, НАД (Ф) — H2—восстановленная и НАД (Ф)— обобщенная формы кофермента никотинамидадениндинуклеотида или никотинамидадениндинуклеотидфосфата.
До момента появления NH3 никаких свободных промежуточных продуктов не обнаружено.
Молекулы мочевины и органических соединений также должны быть подвергнуты соответствующим ферментативным воздействиям, сопровождающимся высвобождением аммиака. Давно была обнаружена способность отдельных представителей прокариотного мира использовать молекулярный азот атмосферы. В последнее время показано, что этим свойством обладают многие прокариоты, принадлежащие к разным группам: эу- и архебактерии, аэробы и анаэробы, фототрофы и хемотрофы, свободноживущие и симбиотические формы. Фиксация молекулярного азота также приводит к восстановлению его до аммиака.
Потребности в источниках серы и фосфора
Сера входит в состав аминокислот (цистеин, метионин), витаминов и кофакторов (биотин, липоевая кислота, кофермент А и др.), а фосфор — необходимый компонент нуклеиновых кислот, фосфолипидов, коферментов. В природе сера находится в форме неорганических солей, главным образом сульфатов, в виде молекулярной (элементной) серы или входит в состав органических соединений. Большинство прокариот для биосинтетических целей потребляют серу в форме сульфата, который при этом восстанавливается до уровня сульфида. Однако некоторые группы прокариот не способны к восстановлению сульфата и нуждаются в восстановленных соединениях серы. Основной формой фосфора в природе являются фосфаты, которые и удовлетворяют потребности прокариот в этом элементе.
Необходимость ионов металлов
Всем прокариотным организмам необходимы металлы, которые могут использоваться в форме катионов неорганических солей. Некоторые из них (магний, кальций, калий, железо) нужны в достаточно высоких концентрациях, потребность в других (цинк, марганец, натрий, молибден, медь, ванадий, никель, кобальт) невелика. Роль перечисленных выше металлов определяется тем, что они входят в состав основных клеточных метаболитов и, таким образом, участвуют в осуществлении жизненно важных функций организма.
Потребность в факторах роста
Некоторые прокариоты обнаруживают потребность в одном каком-либо органическом соединении из группы витаминов, аминокислот или азотистых оснований, которое они по каким-то причинам не могут синтезировать из используемого источника углерода. Такие органические соединения, необходимые в очень небольших количествах, получили название факторов роста. Организмы, которым в дополнение к основному источнику углерода необходим один или больше факторов роста, называют ауксотрофами, в отличие от прототрофов, синтезирующих все необходимые органические соединения из основного источника углерода.
СИНТЕЗ ПРОКАРИОТАМИ ОСНОВНЫХ КЛЕТОЧНЫХ КОМПОНЕНТОВ
Как уже отмечалось выше, основная масса органических веществ клетки состоит из полисахаридов, липидов, белков и нуклеиновых кислот, являющихся (за исключением липидов) полимерами. Образованию полимеров предшествует синтез составляющих их мономеров. В случае полисахаридов — это различные моносахара, нуклеиновых кислот — рибо- и дезоксирибонуклеотиды, белков — аминокислоты.
Биосинтез углеводов
Если прокариоты выращивать на средах, где источник углерода — одно-, двух- или трехуглеродные соединения, то необходимые сахара (в первую очередь C6) они должны синтезировать из имеющихся в среде источников углерода. У подавляющего большинства автотрофов на среде с CO2 в качестве единственного источника углерода сахара синтезируются в реакциях восстановительного пентозофосфатного цикла. У гетеротрофов на среде с C2- и C3-соединениями для синтеза необходимых сахаров используются в значительной степени реакции, функционирующие в катаболическом потоке, например в гликолитическом пути. Однако поскольку некоторые ферментативные реакции этого пути необратимы, в клетках гетеротрофных прокариот, способных использовать двух- и трехуглеродные соединения, сформировались специальные ферментативные реакции, позволяющие обходить необратимые реакции катаболического пути.
Процесс, обеспечивающий синтез C6-углеводов из неуглеводных предшественников, например аминокислот, глицерина, молочной кислоты, получил название глюконеогенеза. Таким путем, сочетающим использование имеющегося в клетке катаболического аппарата и специальных реакций, служащих только для биосинтетических целей, решается прокариотами проблема биосинтеза необходимых моносахаров.
Биосинтез липидов
У прокариот липиды входят в состав клеточных мембран и клеточной стенки, служат запасными веществами, являются компонентами пигментных систем и цепей электронного транспорта. Ниже мы рассмотрим синтез жирных кислот и фосфолипидов, являющихся у большинства прокариот, относящихся к эубактериям, универсальным компонентом клеточных мембран.
C14-C18-жирные кислоты синтезируются путем последовательного присоединения двухуглеродных фрагментов к активированной C2-группе, выполняющей функцию затравки, и последующего восстановления окисленных углеродных атомов.
В клетках эубактерий компонентами липидов являются в основном насыщенные жирные кислоты или содержащие одну двойную связь (мононенасыщенные). Полиненасыщенные жирные кислоты, содержащие две и более двойных связей, найдены до сих пор только у цианобактерий. Образование двойных связей в молекуле кислоты может происходить двумя путями. Один из них, обнаруженный у аэробных эубактерий, требует участия молекулярного кислорода. У облигатно анаэробных и некоторых аэробных эубактерий двойные связи вводятся в молекулу кислоты на ранней стадии ее синтеза в результате реакции дегидратации.
Пути, ведущие к синтезу фосфолипидов, состоят из нескольких этапов. Исходным субстратом служит фосфодиоксиацетон (промежуточное соединение гликолитического пути), восстановление которого приводит к образованию 3-фосфоглицерина. К последнему затем присоединяются два остатка жирных кислот. Продуктом реакции является фосфатидная кислота. Активирование ее с помощью ЦТФ и последующее присоединение к фосфатной группе серина, инозита, глицерина или другого соединения приводят к синтезу фосфатидилсерина, фосфатидилинозита и фосфатидилглицерина соответственно (см. рис. 14).
Биосинтез аминокислот
Большинство прокариот способны синтезировать все аминокислоты, входящие в состав клеточных белков. В качестве исходных углеродных скелетов для биосинтеза аминокислот служит небольшое число промежуточных соединений различных метаболических путей (табл. 10). Введение в молекулу некоторых из них (щавелевоуксусной, a-кетоглутаровой, пировиноградной кислот) аминного азота приводит к образованию аспарагиновой, глутаминовой кислот и аланина. Однако в большинстве случаев исходные соединения должны подвергнуться значительным перестройкам, чтобы сформировать углеродный остов молекулы будущей аминокислоты.
Таблица 10. Некоторые особенности биосинтеза аминокислот
| Предшественник | Метаболический путь, приводящий к образованию предшественника | Аминокислоты с общими биосинтетическими путями |
| Щавелевоуксусная кислота | цикл трикарбоновых кислот реакции карбоксилирования |
аспарагиновая кислота аспарагин лизин метионин треонин изолейцин |
| a-Кетоглутаровая кислота | цикл трикарбоновых кислот | глутаминовая кислота глутамин аргинин пролин |
| 3-фосфоглицериновая кислота | гликолиз цикл Кальвина |
серин глицин цистеин |
| Пировиноградная кислота | гликолиз путь Энтнера-Дудорова |
аланин валин лейцин |
| Фосфоенолпировиноградная кислота + Эритрозо-4-фосфат |
гликолиз окислительный пентозофосфатный путь |
триптофан тирозин фенилаланин |
| 5-Фосфорибозил-1-пирофосфат + АТФ |
окислительный пентозофосфатный путь | гистидин |
Особенностью биосинтеза аминокислот является использование общих биосинтетических путей. Так, 19 из 20 аминокислот, входящих в состав белков, можно по способу их происхождения разделить на 5 групп. Только одна аминокислота (гистидин) образуется по отдельному биосинтетическому пути. Азот вводится в молекулу аминокислоты посредством реакций аминирования, амидирования и переаминирования. Реакции аминирования приводят к образованию из пировиноградной кислоты аланина, а из a-кетоглутаровой — глутаминовой кислоты, например:

|
Две реакции амидирования ведут к образованию глутамина и аспарагина из глутаминовой и аспарагиновой кислот в реакциях следующего типа:
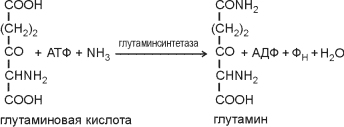
|
где Фн — неорганический фосфат. Глутаминовая кислота и глутамин прямо или косвенно служат донорами амино- и амидогрупп при синтезе практически всех аминокислот и других азотсодержащих органических соединений. Аспарагин используется только для синтеза белковых молекул. Во все остальные аминокислоты азот вводится посредством реакций переаминирования, катализируемых соответствующими аминотрансферазами, при этом во всех реакциях одним из участников является глутаминовая кислота:
глутаминовая кислота + щавелевоуксусная кислота ® аспарагиновая кислота + a-кетоглутаровая кислота.
Еще одним путем включения азота аммиака в состав органических соединений является реакция, приводящая к образованию карбамоилфосфата:

|
Дальнейшее использование азота карбамоилфосфата происходит по двум путям: для синтеза пиримидинов и аргинина.
Биосинтез мононуклеотидов
Из мононуклеотидов построены нуклеиновые кислоты (РНК, ДНК) клеток. Кроме того, мононуклеотиды входят в состав многих коферментов и участвуют, таким образом, в осуществлении различных каталитических функций. Центральное место в биосинтезе мононуклеотидов занимает синтез пуриновых и пи-римидиновых азотистых оснований. Большинство прокариот способно к синтезу этих соединений de novo из низкомолекулярных предшественников. Синтез пуриновых и пиримидиновых мононуклеотидов осуществляется независимыми путями. В результате последовательных ферментативных реакций при синтезе пуриновых нуклеотидов образуется инозиновая кислота, из которой путем химических модификаций пуринового кольца синтезируются адениловая (АМФ) и гуаниловая (ГМФ) кислоты.
Первым пиримидиновым нуклеотидом, синтезируемым de novo, является оротидиловая кислота, декарбоксилирование которой приводит к образованию уридиловой кислоты (УМФ). Последняя служит предшественником цитидиловых нуклеотидов, но соответствующее превращение происходит только на уровне трифосфатов, поэтому сначала из УМФ образуется УТФ, аминирование которого приводит к возникновению ЦТФ.
Дезоксирибонуклеотиды образуются в результате восстановления соответствующих рибонуклеотидов на уровне дифосфатов (для некоторых прокариот описано подобное превращение на уровне трифосфатов). Синтез специфического для ДНК нуклеотида — тимидиловой кислоты — происходит путем ферментативного метилирования дезоксиуридиловой кислоты.
Многие прокариоты способны использовать содержащиеся в питательной среде готовые пуриновые и пиримидиновые основания, их нуклеозиды и нуклеотиды, имея ферменты, катализирующие следующие этапы взаимопревращений экзогенных пуриновых и пиримидиновых производных:
азотистое основание « нуклеозид « нуклеотид (моно- « ди- « трифосфат).
М.В.Гусев, Л.А.Минеева © 1992-2001
Кафедра клеточной физиологии и иммунологии биологического факультета МГУ им. М.В.Ломоносова © 2000-2001
Страница обновлена 09.09.01
Оформление: А.В.Киташов